Машинное обучение в медицине
Диагностика заболеваний по результатам рентгенологических и УЗИ исследований
Диагностика по изображению
В диагностике заболеваний есть большое количество задач, которые можно решить при помощи машинного обучения. В основном задача любой модели сводится к предсказанию, болен ли человек сейчас.
В задаче предсказания наличия болезни используются чаще всего глубокие нейронные сети, которые на вход получают картинку с рентгенологическим или ультразвуковым исследованием пациента и по ним предсказывают наличие болезни. Большое распространение такой подход получил в задаче предсказания злокачественности опухоли. За основу часто берут GoogleLeNet[1], при этом точность предсказаний превышает 90%. Такие модели учатся на размеченных тренировочных наборах данных, поэтому их можно отнести к обучению с учителем.
Применения
Поскольку точность предсказаний у таких моделей достаточно высока, их стали применять на практике. Сейчас ведутся исследования по внедрению таких моделей в УЗИ-аппараты для того, чтобы быстрее и точнее определять местоположение и злокачественность опухоли. Кроме того, такие модели стали применять в направленной лучевой терапии, когда злокачественная опухоль облучается различными видами частиц. Известно, что эти частицы уничтожают не только раковые, но и здоровые клетки. Именно поэтому активно внедряются модели, которые могут подсказать аппарату точное направление облучения.
Персонализированная медицина
Персонализированная медицина — новая организационная модель построения медицинской помощи пациентам, которая основывается на подборе индивидуальных лечебных, диагностических и превентивных средств, оптимально подходящих по биохимическим, физиологическим и генетическим особенностям организма.
Основная цель нового направления в медицине заключается в персонализации и оптимизации профилактических мероприятий и лечения пациентов для исключения негативных последствий и осложнений, проявляющихся из-за индивидуальных особенностей. Основные отрасли медицины, где применяются новые принципы — онкология, фармация и фармакогеномика. Последняя занимается изучением реакций организма на медицинские препараты в зависимости от индивидуальных наследственных факторов.
Экспрессия генов
Многие модели ориентируются на данные экспрессии генов (в широком смысле — процесс получения белка из последовательности ДНК). Известно, что от количества белков напрямую зависит возможность клеток становиться раковыми, а также порождать любые другие заболевания. Совокупность изменений в большом количестве различных белков может приводить к заболеванию. Именно поэтому модели персонализированной медицины основываются на данных экспрессии.
Медицинская карта
Другая задача — предсказать, заболеет ли человек в будущем. Для этого часто используется медицинская карта пациента, и на вход сети подаются данные о пациенте, результаты исследований, его генеалогическое древо и другая медицинская информация. Основываясь на полученных данных, модель должна предсказать вероятность того, что человек может заболеть каждым из приведенного набора болезней. Если вероятность хотя бы по одному из маркеров превышает некоторое значение — такая модель рекомендует пациенту обратиться к специалисту. В свою очередь специалист может подтвердить или же опровергнуть опасения модели, отдавая ей результат — права модель или нет. Таким образом, мы получаем обучение с подкреплением.
Поиск лекарств
Поиск лекарств (англ. drug discovery, drug design) — процесс поиска новых лекарственных средств, часто основанный на знаниях о биологической мишени. При поиске новых лекарстdенных средств часто прибегают к помощи машинного обучения в таких задачах, как предсказание молекулярных свойств потенциальной молекулы лекарства, формы какого-либо белка, активности взаимодействия между двумя молекулами и т.д.
Предсказание молекулярных свойств
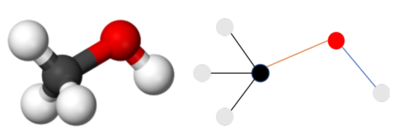
Одна из главных задач машинного обучения при поиске новых лекарств — сужение круга их поиска. Чаще всего фармацевтические компании имеют на руках библиотеки с огромным количеством веществ, которые они потенциально могут синтезировать и опробовать в качестве лекарства. Но обычно размеры этих библиотек составляют тысячи молекул, поэтому синтезировать и проверить каждую из них не представляется возможным. В этом случае прибегают к предсказанию некоторых свойств этих молекул, которые точно определяют, может ли молекула быть использована как лекарство. Для предсказания свойств молекул обычно используют молекулярный граф — графическое представление молекулы (ее атомов и связей).
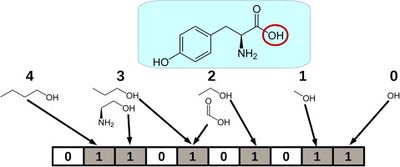
Первые нейронные сети для предсказания молекулярных свойств использовали Моргановские фингерпринты (англ. Morgan fingerpints), которые для каждого атома в молекуле выделяли всех его соседей на каком-то определенном расстоянии (которое является гиперпараметром) и смотрели на наличие такой подструктуры в молекуле. Получался аналог некоторого оne-hot кодирования. Впоследствии этот метод был несколько усовершенствован, и стали смотреть не на наличие подструктуры, а на то, сколько раз она встречается в молекуле. Прорыв в этой области случился с появлением сети NeuralFingerprints [2], где фингерпринты получались путем учета важности подструктур из Моргановских фингерпринтов, то есть были добавлены веса у каждой из возможных подструктур.
Эта сеть была одной из первых в этой области, и сейчас используется как baseline метод в огромном количестве статей. В основу же новых методов сейчас чаще всего ложатся графовые нейронные сети. Подходы графовых нейронных сетей адаптируют под молекулярный граф путем поиска элементов на расстоянии не более, чем N (где N является гиперпараметром), или последовательным рассмотрением каждой вершины и усреднением полученых значений.
Предсказание формы белка

Секвенирование — процесс получения нуклеотидной последовательности из молекулы ДНК. [3] Из нуклеотидной последовательности можно получить аминокислотную последовательность, которая в свою очередь кодирует любой белок в организме.
Предсказание формы белка — другая очень важная задача машинного обучения в фармацевтике. С возникновением технологий секвенирования ДНК у сообщества появилась возможность быстро и достаточно качественно прочитывать белковые последовательности, но получать пространственную структуру полученных белков экспериментально все еще очень трудоемко и дорого. Пространственная же структура белка важна для генерации мишеней, поэтому задача предсказания структуры является очень важной. Например, при подборе потенциальной вакцины, необходимо точно знать форму антитела, чтобы понимать сможет ли это соединение захватить свою мишень, не дав ей закрепиться в организме пациента.
Предсказание формы белков основано на нейронных сетях, которые как вход используют очень длинную аминокислотную последовательность (размер алфавита ограничен - всего различных аминокислот 20), а на выходе должны предсказать значения торсионных углов[4] между аминокислотами. В декабре 2020 года DeepMind (исследовательское подразделение Google) заявили, что решили проблему пространственной структуры белка.[5] Авторы модели утверждают, что значение метрики глобального расстояния (англ. global distance test) превысило 90%. Метрика глобального расстояния — это метрика, которая вычисляется для каждой аминокислоты как процент атомов углерода из главной цепи белка, которые в сгенерированном белке расположены не более чем на расстоянии какого-то определенного количества ангстрем от соответствующего атома углерода в исходном белке. Обычно это значение берется равным 1, 2, 4 или 8 ангстрем (10-10м).